МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ для выполнения лабораторной работы по физической химии «Закон распределения. Жидкостная экстракция»
Страница 3 из 5
По формуле (6) в воде осталось йода:
Б)  Г
Г
Это составляет: 
Значит, в слой ССI4 извлекается 100 – 8,45 = 91,55 %
Вывод: Многократная экстракция ведет к повышению извлечения.
II. ПРАКТИЧЕСКАЯ ЧАСТЬ.
Опыт № 1. Определение степени ассоциации уксусной кислоты в органическом растворителе.
Уксусная и другие карбоновые кислоты в органическом растворителе ассоциированы за счет водородных связей. В то же время их диссоциация в воде мала и ею можно пренебречь.
Поэтому для расчета коэффициента распределения можно воспользоваться формулой:
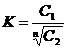 ,
, 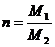 ,
,
Где М1, М2 – молекулярные массы растворенного вещества в ассоциированном и мономолекулярном виде.
В логарифмической форме:
Lg C2 = n lg C1 – lg K
Цель работы: 1. Определение равновесных концентраций СН3СООН в воде и хлороформе (или экстракционном бензине).
2. Расчет коэффициента распределения:
А) по формуле (1)
Б) по формуле (2)
В) графически.
На основе математического выражения К сделать вывод о состоянии молекул уксусной кислоты в органическом растворителе.
3. Расчет (%) СН3СООН в органической фазе.
Оборудование и реактивы:
Растворы СН3СООН 1,5; 1,0; 0,5 Н; растворы NaOH для титрования:
0,5 Н NaOH – титрование водной фазы;
0,02 Н NaOH – титрование органической фазы;
Индикатор – фенолфталеин, спиртовой раствор;
Хлороформ или экстракционный бензин.
Делительные воронки (100 мл), 3 шт. бюретки – 2 шт., конические колбы для титрования, встряхиватель.
Ход работы:
1. Приготовить 3 раствора СН3СООН: 1,5 1,0 и 0,5 Н
2. В делительные воронки емкостью 100 мл отобрать по 25 мл каждого раствора.
3. В каждую воронку добавить 25 мл СНСl3.
4. Воронки плотно закрыть и интенсивно встряхивать 20 минут, изредка открывая пробку.
5. Оставить воронки в покое до полного расслаивания фаз.
6. Слить нижний слой, открывая сначала пробку, а затем кран.
7. Отобрать пипеткой по 5 мл равновесного водного раствора и оттитровать 0,5 Н раствором NaOH по фенолфталеину (3 параллельных определения!).
8. Пробы из органической фазы отобрать пипеткой на 5 мл с помощью груши. Добавить 15-20 мл дистиллированной воды и оттитровать 0,02 Н по фенолфталеину до неисчезающей слабо-розовой окраски.
9. Результаты свести в таблицу:
|
№ раст-вора
|
VNaOH, мл
|
VNaOH, мл
|
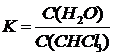
|
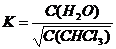
|
|
Водный слой
|
С(Н2О)
|
Органический
|
С(СНСl3)
|
|
1
|
2
|
3
|
1
|
2
|
3
|
|
1
2
3
|
|
|
|
|
|
|
|
|
|
|
10. Найти значение n и К графически (см. пример 1).
Опыт 2. Изучение процесса экстрагирования.