МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ к лабораторной работе по физической химии ПРИМЕНЕНИЕ МЕТОДОВ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА В ХИМИЧЕСКОЙ КИНЕТИКЕ
Страница 7 из 11
Реакция протекает бимолекулярно в разбавленном водном растворе практически до конца.
Для реакций второго порядка
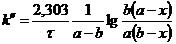 (3.1),
(3.1),
Где 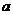 - начальная концентрация первого вещества,
- начальная концентрация первого вещества, 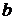 - начальная концентрация второго вещества,
- начальная концентрация второго вещества, 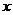 - количество вещества, вступившее в реакцию к моменту времени
- количество вещества, вступившее в реакцию к моменту времени 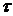 от начала опыта.
от начала опыта.
Если начальные концентрации одинаковы, т. е. 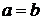 , то после интегрирования уравнение принимает более простой вид:
, то после интегрирования уравнение принимает более простой вид:
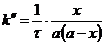 (3.2).
(3.2).
Уравнение для удельной теплопроводности 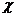 смеси электролитов имеет вид:
смеси электролитов имеет вид:
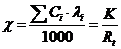 (3.3),
(3.3),
Где 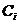 - концентрация
- концентрация 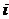 -го иона,
-го иона, 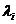 - подвижность
- подвижность 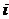 -го иона,
-го иона, 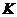 -
- 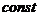 сосуда,
сосуда, 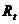 - измеренное сопротивление раствора.
- измеренное сопротивление раствора.
Электропроводность 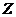 раствора, равная
раствора, равная 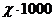 , связана с концентрацией уравнением
, связана с концентрацией уравнением
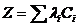 (3.4)
(3.4)
Применяя уравнение (3.4) для реакционной смеси, получим одновременно три уравнения.
Первое – для начала реакции, когда в растворе присутствуют только ионы 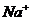 и
и 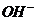 . В этом случае электропроводность
. В этом случае электропроводность 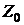 соответствует электропроводности
соответствует электропроводности 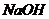 начальной концентрации:
начальной концентрации:
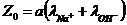 .
.
Второе уравнение для конца реакции, когда в растворе присутствуют только ионы 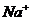 и
и 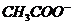 ; здесь
; здесь
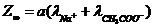 .
.
Третье уравнение для электропроводности раствора ко времени 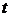 , когда в растворе находятся все три иона.
, когда в растворе находятся все три иона.
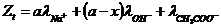 .
.
Величину 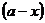 для разбавленных растворов можно выразить через
для разбавленных растворов можно выразить через 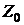 ,
, 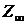 и
и 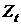 :
:
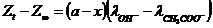 ;
;
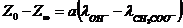 , откуда
, откуда
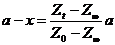 (3.5).
(3.5).
Заменяя 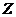 измеренными значениями сопротивления
измеренными значениями сопротивления 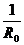 ,
, 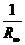 ,
, 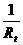 и
и 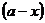 , получим уравнение для реакции второго порядка:
, получим уравнение для реакции второго порядка:
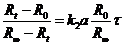 или
или
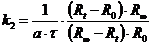 (3.6).
(3.6).
3.2 Экспериментальная часть.
Цель работы: Определение порядка реакции, константы скорости, энергии активации и предэкспоненциального множителя при омылении этилацетата едким натром.
Приборы и реактивы: электролитическая ячейка для проведения кондуктометрических измерений, реохордный мост.