МЕТОДИЧЕСКИЕ УКАЗАНИЯ по выполнению лабораторно-практических занятий по дисциплине «Физическая и коллоидная химия» «Гетерогенные равновесия. Фазовые диаграммы температура кипения - состав для двухкомпонентных систем»
Страница 4 из 9
[ pKq+] [ qLp-] ↔ pKq+ + qLp-
Рассмотрим некоторые виды фазовых диаграмм двухкомпонентных систем.
А) Системы с неограниченной взаимной растворимостью компонентов.
Однофазные двойные жидкие системы
Такие системы характерны для случая, когда вещества, образующие систему, обладают достаточно близкими физическими параметрами (состав, структура, наличие дипольного момента…). Это могут быть смеси изомеров или гомологов, обладающие близкими химическими свойствами и структурой. При этом силы взаимодействия между разнородными частицами А - В, примерно равны межмолекулярным взаимодействиям между одинаковыми частицами А - А и В – В. Образование раствора в этом случае происходит без изменения объема и без заметного выделения тепла.
Для изучения равновесий в гомогенных жидких системах применяются методы, основанные на изучении концентрационной зависимости от следующих групп свойств:
*механические – плотность, вязкость;
*поверхностные – поверхностное натяжение;
*оптические – показатель преломления;
*спектральные – оптическая плотность или интегральная интенсивность полос поглощения в различных областях спектра;
*электрические – электропроводность, диэлектрическая проницаемость и т. д.
Из перечисленных параметров свойством аддитивности обладают плотность, показатель преломления, оптическая плотность.
Рассмотрим зависимость температуры кипения от состава смеси в изобарном процессе (Р = const) (Рис.2.3):

Рис. 2.3. Диаграмма кипения двухкомпонентной смеси с неограниченной взаимной растворимостью компонентов.
Диаграмма кипения имеет две кривые, разделяющие ее на 3 области:
*Область пара: V(усл.) = 2 – 1 + 1 = 2
*Область жидкости: V(усл.) = 2 - 1 + 1 = 1
*Область равновесия между паром и жидкостью: V(усл.) = 2 – 2 + 1 = 1 (Только один параметр - температура или состав смеси может быть выбран произвольно. Каждому значению температуры отвечают строго определенные значения равновесного состояния жидкость - пар).
ТА и ТВ – фигуративные точки, отражающие температуры кипения чистых жидкостей.
Фигуративные точки, лежащие на нижней кривой (кривая кипения жидкости), характеризуют составы кипящих жидкостей и температуры, при которых начинают кипеть жидкие смеси при постоянном давлении.
Фигуративные точки, лежащие на верхней кривой (кривая конденсации пара), характеризуют составы насыщенного пара и температуры, при которых исчезают последние капли жидкости при кипении исходных смесей.
Фигуративные точки, расположенные между двумя кривыми, отражают ситуацию, когда состав жидкой смеси не совпадает с составом равновесной ей паровой смеси. При этом равновесные составы лежат на линии Т = const, соединяющей точки равновесных фаз. Такая линия называется нодой или конодой. Состав парожидкостной смеси Х легко определить графически, проведя ноду через точку Х. При этом количественные соотношения фаз находят по правилу рычага.
Подобные системы имеют большое практическое значение для расчета процессов фракционной перегонки и ректификации.
Б. Системы с взаимно нерастворимыми или ограниченно растворимыми компонентами - двухфазные двойные жидкие системы
Подобные системы характерны для жидкостей, практически нерастворимых друг в друге: бензин – вода, бензол – вода, эфирные масла – вода и др. Вид диаграммы состояния – диаграммы кипения такой системы приведен на рис.2.4:
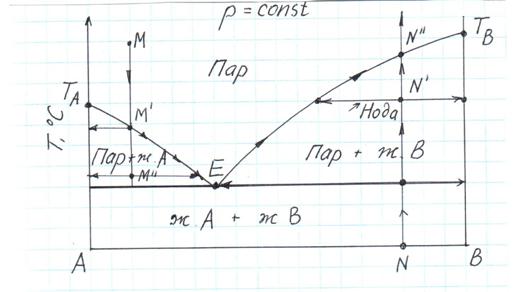
Рис. 2.4. Диаграмма кипения двух взаимно нерастворимых жидкостей.
Смесь взаимно нерастворимых жидкостей двухфазна при любых соотношениях компонентов. Так как жидкие фазы – это практически чистые жидкости, общее давление паров над ними равно сумме парциальных давлений:
Р = рА0 + рВ0.