МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ к лабораторной работе по физической химии ПРИМЕНЕНИЕ МЕТОДОВ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА В ХИМИЧЕСКОЙ КИНЕТИКЕ
Страница 8 из 11
Растворы: 100 мл 0,01 н 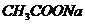 и 100 мл 0,05 н
и 100 мл 0,05 н 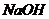 , 0,2 М
, 0,2 М 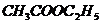 (1,762 г / 100 мл).
(1,762 г / 100 мл).
Ход работы.
J В чистый сосуд для измерения электропроводности ввести 2 мл 0,05 н 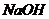 + 8 мл
+ 8 мл 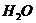 . Вставить промытые, сухие электроды и после термостатирования (15 мин) при 25°С измерить
. Вставить промытые, сухие электроды и после термостатирования (15 мин) при 25°С измерить 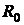 .
.
K Измерить 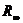 0,01 М
0,01 М 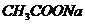 .
.
L В сухой сосуд влить из бюретки 4 мл 0,05 н 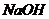 , 15 мл
, 15 мл 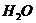 , вставить электроды, термостатировать 15 мин. Затем добавить 1 мл 0,2 М этилацетата, перемешать и отметить по секундомеру момент смешивания растворов как время начала реакции.
, вставить электроды, термостатировать 15 мин. Затем добавить 1 мл 0,2 М этилацетата, перемешать и отметить по секундомеру момент смешивания растворов как время начала реакции.
M Измерять 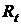 через 1, 2, 4, 6, 10, 15, 20 мин после смешивания.
через 1, 2, 4, 6, 10, 15, 20 мин после смешивания.
N Результаты записать в таблицу по форме:
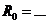 ,
, 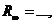
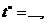
|
Время
|
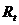 , Ом , Ом
|
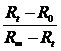
|
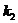
|
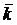
|
|
По
Часам
|
От начала опыта 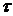 , мин , мин
|
|
|
|
|
|
|
O Повторить эксперимент при другой температуре.
P Обработать результаты эксперимента:
A) Рассчитать константу скорости по уравнению (3.6).
B) Рассчитать константу скорости графически по кривой зависимости 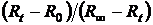 от времени
от времени 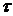 .
.
C) Энергию активации 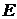 и предэкспоненциальный множитель
и предэкспоненциальный множитель 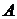 найти графически по длине отрезка
найти графически по длине отрезка 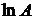 и углу
и углу 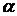
Уравнение Аррениуса:
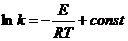 или
или 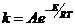 .
.
3.3 Задачи для самостоятельного решения.
1. Константа скорости омыления этилового эфира уксусной кислооты едким натром при 10°С 2,38. определить время (мин), необходимое для омыления 90 % эфира, если смешать при 10°С 1 л 0,05 н раствора эфира с :
1) 1 л 0,05 н 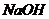 ;
;
2) 1 л 0,1 н 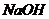 .
.
Решение.
1) Реакция омыления эфира щелочью является реакцией второго порядка. В первом случае, когда концентрации эфира и щелочи равны, выражение для константы скорости:
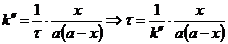
Общий объем смеси 2 л, поэтому концентрация вещества 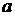 вследствие разбавления уменьшится вдвое:
вследствие разбавления уменьшится вдвое:
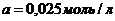 ;
;
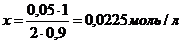
(учитываем разбавление в 2 раза и омыление на 90 %)